botnání gelů polyelektrolytů
swelling of polyelectrolyte gels
Pohlcování nízkomolekulárního rozpouštědla reverzibilním xerogelem, jehož síťovitá struktura je tvořena
polyelektrolytem.
Botnání těchto gelů je do značné míry ovlivněno přítomností elektrolytů a hodnotou pH roztoku. Stejně jako u
osmózy se i zde uplatňují
membránové rovnováhy. Nabotnalý gel ve styku s vodným roztokem může být přirovnán k roztoku polyelektrolytu, který je od vodné fáze oddělen
polopropustnou membránou. Vysokomolekulárním iontem je zde řetězec mezi dvěma spoji, roli membrány má síťovitá struktura gelu.
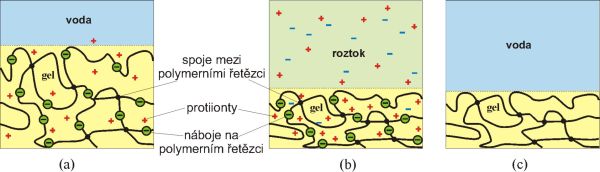
V čisté vodě jsou v síťovité struktuře botnajícího gelu přítomny malé ionty, vzniklé disociací postranních skupin řetězce (obr. 1a). Vzhledem k podmínce elektroneutrality může do vody přejít jen velmi málo protiiontů. Velký rozdíl koncentrací protiiontů v gelu a ve vodě zvyšuje snahu molekul vody přecházet do gelu. Botnavost tohoto gelu je mnohem vyšší než u gelu stejné struktury, který nedisociuje (obr. 1c) (botnací tlak se zvyšuje o osmotický tlak odpovídající přítomnosti protiiontů v gelu).
Je-li ve vodné fázi přítomen nízkomolekulární elektrolyt (obr. 1b), uplatňují se membránové rovnováhy opačně: v rovnováze je koncentrace nízkomolekulárního elektrolytu v gelu menší, než v jaké zůstává v okolním kapalném roztoku a celková hodnota botnacího tlaku se zmenšuje; při velké koncentraci nízkomolekulárního elektrolytu klesne botnací tlak až na hodnotu odpovídající nedisociovanému gelu (obr. 1c). Stejně je ovlivněna i afinita k botnání a rovnovážný stupeň nabotnání.
 |
|
Obr. 1 Botnání gelu vysokomolekulárního elektrolytu
(a) v čisté vodě; botnací tlak se zvyšuje o osmotický tlak oddisociovaných protiiontů
(b) v roztoku nízkomolekulárního elektrolytu
(c) nedisociovaný gel stejné struktury v čisté vodě
|
Grafy souvislostí do úrovně:
I  II
II